Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
«GLYSOCAL» PILLS PREPARATION AND STUDY OF THEIR BIOPHARMACEUTICAL CHARACTERISTICS
В настоящее время актуальной проблемой фармацевтической технологии является изготовление фитогранул содержащих экстракты из сбора растений и используемых для профилактики и лечении гастроэнтерологических заболеваний.
Методы исследования. Была разработана технология получения гранул из очищенного экстракта, фитосбора «Glysocal», состав которого богат флаваноидами и тритерпеновыми гликозидами [1]. При изготовлении гранул вспомогательные вещества надо было выбрать так, чтобы они усиливали ранозаживляющий эффект главного действующего компонента. С этой целью было целесообразно использовать природный полимер - хитозан [4, 6]. Далее мы использовали как склеивающе-связывающее средство - экстракт прополиса, так как экстракт прополиса обладает высокой адгезивностью, а также имеет богатый состав: флавоноиды и прочие вещества широко используемые при лечении язвенной болезни ЖКТ [5, 7]. При приготовлении гранул были использованы различные количества экстракта прополиса, состав гранул был сконструирован в трех композициях. 1 композиция: сумма БАВ фитосбора «Glysocal» -3,0 г, магнезиум карбонат основной - 1,5 г, экстракт прополиса -
0,5 г, хитозан - 7,0г, аеросил 0,5 г, спирт этиловый 70%-10мл, сахар - 77,5 г; 2- композиция: сумма БАВ из фитосбора «Glysocal» -3,0 г, магния карбонат основной - 1,5 г, экстракт прополиса - 1,5 г, хитозан - 7,0 г, аэросил 0,5 г, спирт этиловый 70%-10мл, сахар - 76,5 г; 3- композиция: сумма БАВ из фитосбора «Glysocal»-3,0г, магния карбонат основной - 1,5 г, экстракт прополиса - 2,5 г, хитозан - 7,0 г, аэросил 0,5 г, спирт этиловый 70%-10мл, сахар - 75,5 г.
Были установлены некоторые технологические особенности фитогранул «Glysocal»: определены органолептические свойства, количество БАВ в их составе, влажность, время распадаемости. Проведенный анализ выявил, что используемый экстракт прополиса в зависимости от количества действует по-разному на устойчивость гранул. Гранулы приготовленные из
1 композиции, которая содержит 0,5% экстракт прополиса распадаются соответственно в течении 5 и 7 минут (табл. 1).
Гранулы, приготовленные из 1 и 3 композиций распадаются в течение соответственно 5,2±0,037 и 15,0±0,55 минут (это в искусственном соке), в кишечном соке в течение 7,0±0,45 и 19,2±0,58 минут. При такой разнице гидрофобная природа прополиса имеет решающее значение. Из-за повышения количества прополиса в составе гранул усиливается гидрофобность массы, и поэтому гранулы, приготовленные из
3-й композиции, распадаются в течение длительного времени. В результате проведенных исследований было установлено, что гранулы, приготовленные из 2 композиции [3], в большей степени отвечают требованиям, предъявляемым к ним. При проведении теста «растворение» (прибор «Вращаюшая корзинка», скорость вращение
200 об/мин, среды растворения 1000 мл)
2 композиции определяли оптимальные условия: среда pH-7.8, объем среды растворения 500 мл, скорость вращения прибора - 100 об/мин. Расворение гранул «Glysocal» происходит интенсивнее в условиях кищечника за 45 минут растворяется 88% действующих веществ, в то время как в среде исскусственного желудочного сока растворяется 75% действующих веществ.
Таблица 1.
Некторые технологические показатели гранулы «Glysocal»
|
Композиции |
Описание |
Влажность, % |
Количество |
Распадаемость, минут
|
|||
|
Рутин |
Глицир-ризиновая кислота |
pH-1,0 |
pH-8,0 |
Вода очищенная |
|||
|
1 композиция М±м Min-max |
Светло-желтый, запах специфический |
2,21±0,03 2,12-2,29 |
9,40±0,05 9,20-9,50 |
8,22±0,07 8,0-8,40 |
5,2±0,037 4,0-6,0 |
7,0±0,45 6,0-8,0 |
32,2±0,97 29,0-34,0 |
|
2 компо-зиция М±м Min-max |
Желтый, запах специфический |
2,18±0,03 2,1-2,27 |
9,54±0,07 9,40 -9,80 |
8,34±0,1 8,0-8,50 |
8,0±0,55 6,0-9,0 |
10,4±0,6 9,0-12,0 |
40,0±1,14 36,0-43,0 |
|
3 компо-зиция М±м Min-max |
Светло-желтый, запах специфический |
2,2±0,03 2,11-2,28 |
9,46±0,04 9,4-9,6 |
8,26±0,08 8,10-8,50 |
15,0±0,55 13,0-16,0 |
19,2±0,58 18,0-21,0 |
58,0±1,76 55,0-64,0 |
Обсуждения и результаты
Изучение биофармацевтических особенностей гранул «Glysocal» было проведено в опытах in vitro, in situ и in vivo. В опытах in vitro был использован метод диализа через целлофановую мембрану. В качестве среды диализа был выбран искусственный кишечный и искусственный желудочный сок. Исследования проводились в обеих средах. В этих средах были изучены скорость отделения растворенного рутина от искусственной мембраны. С этой целью, гранулы растворялись в 10 мл буферного раствора (pH=1,0), и добавлялись в пробирку. Далее ее закрывали целлофановой мембраной и помещали в химический стакан с раствором Рингера, после чего аппарат ставили в термостат. Наряду с взятием 5 мл раствора из диализата каждые 30 минут, в диализат добавляли в том же объеме новый раствор Рингера. Взяв 5 проб из диализата, их помещали в фарфоровую чашку и выпаривали. Полученный сухой остаток растворяли с 95% этиловым спиртом, процеживали в чистый флакон. Фильтр промывали 95% этиловым спиртом. Объем доводили до 8 мл. Затем проводили количественный анализ рутина спектрофотометрометрически [2]. А во втором опыте исследования проводились в среде pH=8,0. С этой целью в пробирку добавляли по 2 г гранул и 10 мл искусственного кишечного сока и растворяли, затем закрывали целлофановой мембраной. Опыты повторялись. Из результатов проведенных исследований в выбранных модельных системах видно, что в выбранных модельной системе искусственного желудочного сока, процесс высвобождения и всасывания действующих веществ из гранул происходит в течение 50 минут. После этого, максимальное количество БАВ, конкретно рутина, проходящего в диализат, происходит в течение 120 минут (67 мкг/мл). После этого времени повышение количества рутина в диализате не наблюдается. Аналогично процесс наблюдается в другой модельной системе. Здесь всасывание рутина происходит в течение 30 минут. Максимальное накопление рутина в диализате (74,5 мкг/мл) происходит в течение 95-100 минут (рис.1). В среде «тонкий кишечник» наряду другими компонентами, растворение рутина происходит хорошо, не образуется масса геля хитозан и оно в отличие от искусственного желудочного сока ускоряет всасывание веществ.
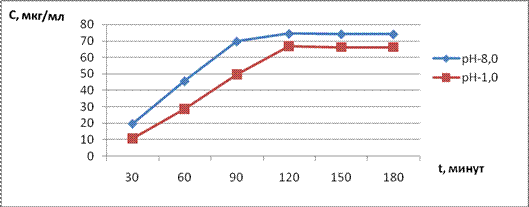
Рис. 1. Скорость высвобождения рутина через целлофановую мембрану из гранул «Glysocal»
Опыты in situ выполнены на отрезке прямой кишки кролика. Для осуществления опыта in vivo брали 10 мл раствора приготовленного из гранул и кормили per os кроликов из породы шиншиллы весом 2 кг. Каждые 15, 30, 60, 90, 120, 150 минут брали по 2 мл крови из ушной вены кролика. Отделение на составные части проводилось в течение 30 минут в центрифуге (3000 об/мин). С истечением времени брали 1 мл отделенной плазмы, перемешиваем в фарфоровую чашку и выпариваем. Полученный сухой остаток растворяли в 95% этиловом спирте, процеживали в чистый флакон из бумажного фильтра. Фильтр промывали 95% этиловым спиртом. Объем доводили до 8 мл. Следующие операции проводили по аналогии с опытом in vitro. Процесс резорбции БАВ в опытах in situ в отличие от опытов in vivo происходит более интенсивно (рис. 2).
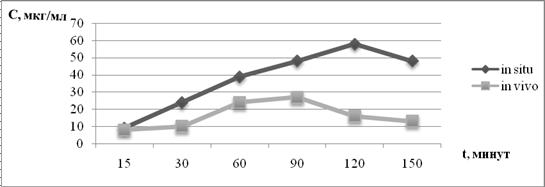
Рис. 2. Скорость высвобождения рутина из гранулы «Glysocal»
(in situ, in vivo опыты)
Так как, через 90 минут количество рутина переходящего в модельную жидкость составляет 58 мкг/мл и повышение количества рутина после этого времени не наблюдается. А в опытах in vivo максимальное количество рутина выделяется из гранул наблюдается в течение 60-90 минут (28 мкг/мл). После этого времени количество рутина в крови постепенно понижается. На 150 минуте концентрация рутина в крови в течение 15 минут равняется количеству рутина переходящего в кровь (13мкг/мл). В отличие от опыта in situ, в опытах in vivo наблюдается через 90 минут понижение количества рутина, что можно объяснить его постепенным метаболизмом в организме.
Выводы:
- Способом влажной грануляции получены фитогранулы «Glysocal» в качестве склеиваюшего вещества был взят 1,5 г экстракта прополиса и изучены некоторые его технологические свойства: распадаемость в очищенной воде 40,0±1,12 в минуту в кислой модельной среде 8,0±0,55; а в щелочной 10,4±0,6 минут; влажность 2,18±0,03%; в условиях кищечника за 45 минут растворяется 88% действующих веществ.
- В опытах in vitro в исскуственной системе «желудок» максимальное количество рутина, проходящего через диализат из фитогранул «Glysocal» в течение 120 минут составило 67 мкг/мл, на моделях системы «тонкий кишечник» - 74,5 мкг/мл в течении 95-100 минут, в опытах in situ 58мкг/мл в течении 90 минут, а в опытах in vivo количество рутина, проходящего через плазму, было 28 мкг/мл в течение
90 минут.
СПИСОК ЛИТЕРАТУРЫ
- Мехралиева С.Д., Велиева М.Н., Тагиев С.А. Патент- АЗ № а 2007 0246 «Способ получения экстрактивных веществ из растительного сырья».
- Мехралиева С.Д. Изучение биофармацевтических свойств геля «Глисотрикал» в эксперименте (in vitro) // Медицинцкий журнал Грузии, 2008, № 4,с.31-34.
- Мехралиева С.Д., Велиева М.Н., Тагиев С.А., Гасанова Д.А. Патент- АЗ № а2008 0051 «Лекарственное средство».
- "Chitosan; Poly-D-glucosamine (128930) Fact Sheet". US Environmental Protection Agency. Retrieved on 2006, p. 23-26.
- Gebaraa EC, Pustiglioni AN, de Lima LA, et al. Propolis extract as an adjuvant to periodontal treatment // Oral Health Prev Dent 2003, Vol. 1(1), p. 29-35.
- Retrieved on 18 February 2008. Retrieved from "http://en.wikipedia.org/wiki-/Chitosan" .
- Santos VR, Pimenta FJ, Aguiar MC, et al. Oral candidiasis treatment with Brazilian ethanol propolis extract // Phytother Res 2005, Vol. 19 (7), p. 652-654.
Библиографическая ссылка
Мехралиева С.Д. ПРИГОТОВЛЕНИЕ ГРАНУЛ «GLYSOCAL» И ИЗУЧЕНИЕ ИХ БИОФАРМАЦЕВТИЧЕСКИХ ОСОБЕННОСТЕЙ // Успехи современного естествознания. 2010. № 5. С. 39-42;URL: https://natural-sciences.ru/en/article/view?id=8109 (дата обращения: 20.05.2026).



